※本資料は各一次文献およびKDIGO 2024ガイドライン等に基づいて構成しています。日本国内での適用にあたっては、最新の添付文書・日本腎臓学会CKD診療ガイド等を併せてご確認ください。
ACE阻害薬と聞いて、まず何を思い浮かべますか。「降圧薬」「腎保護」「空咳に注意」——おそらくこの3つで止まっている方が多いのではないでしょうか。
実際、薬学教育や日常業務の中でACE阻害薬は「腎臓を守る薬」として繰り返し登場します。CKD(慢性腎臓病)の進行抑制、糖尿病性腎症の第一選択、心不全の予後改善——どれも「良い薬」としての顔です。その認識自体は正しい。ただ、その認識だけで止まっていると、ある場面で足をすくわれます。
ACE阻害薬は、条件が重なると急性腎障害(AKI)を引き起こしうる薬剤でもあります。
「腎保護薬なのに腎障害?」——ここ、矛盾しているように見えて、実は機序を押さえれば判断軸がクリアになります。そして、この「腎保護の裏側」を理解しているかどうかが、処方鑑査やシックデイ指導の質を分ける境界線です。
この資料では、一次文献のエビデンスと最新のKDIGO 2024ガイドラインを照合しながら、現場で使えるリスク評価・モニタリング・シックデイ対応のポイントを整理します。「リスク因子のある患者にACE阻害薬が出ている。続けていいのか、止めるべきか」——この判断に迷ったことはありませんか。その迷いを整理するためのフレームワークを、一緒に確認していきましょう。
目次
1. 「腎保護薬」のもう一つの顔——なぜAKIが起こるのか
1-1. 教科書で習った「腎保護」の機序をもう一歩先へ
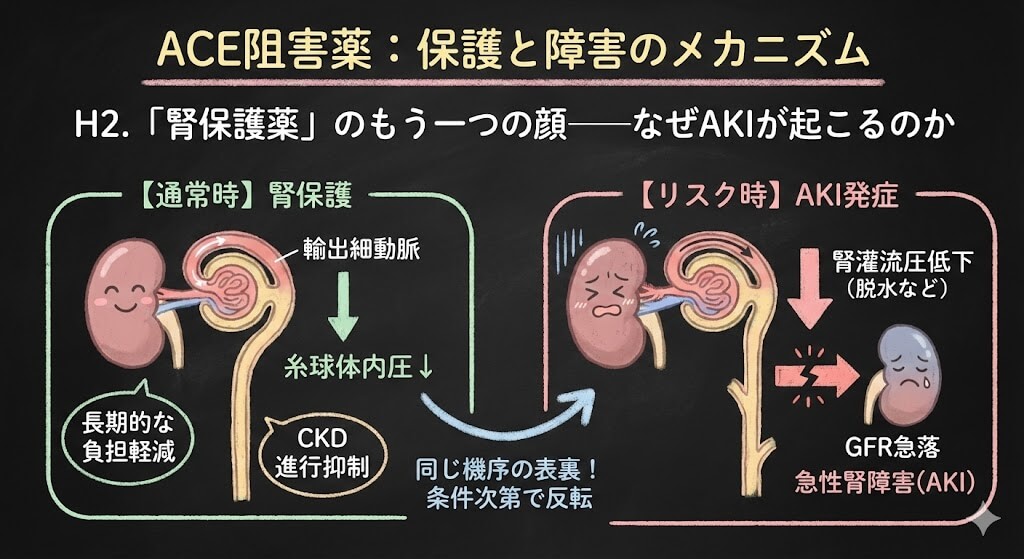
まず機序のおさらいから。ACE阻害薬は輸出細動脈を拡張し、糸球体内圧を下げることで長期的な腎保護効果を発揮します。糸球体の過剰ろ過を抑え、腎臓への負担を減らす。これ自体は「良い作用」であり、REIN試験やAIPRI試験などで蛋白尿の減少・CKD進行抑制のエビデンスが蓄積されてきました(KDIGO 2024 Recommendation 3.6.1)。
ここまでは、多くの薬剤師がご存じのはずです。
問題は、この「輸出細動脈の拡張」という同じメカニズムが、条件次第で腎障害にも振れるという点です。
1-2. 「保護」が「障害」に反転するとき
腎灌流圧がすでに低下している状態——たとえば脱水、低血圧、両側腎動脈狭窄——では話が変わります。このとき糸球体ろ過量(GFR)はアンジオテンシンIIによる輸出細動脈の収縮に強く依存しています。いわば、輸出細動脈の収縮がGFRを辛うじて維持している「最後の砦」です。
ここにACE阻害薬が入ると、その砦が外れ、GFRが急落します(Textor SC, Semin Nephrol 1997; DiBianco R, Med Toxicol 1986)。
つまり、同じ薬理作用が「保護」にも「障害」にもなる。違いは患者側の条件だけです。
つまり、薬が悪いというより”条件の重なり”が問題ってことですか? でも正直、腎保護のイメージが強すぎて、腎障害の方はあまり意識してなかったです…

オカメインコ

ポッポ先生
それは珍しくないです。ACE阻害薬は「腎臓に良い薬」として教わる機会が圧倒的に多いですからね。ただ、NICEガイドラインでも指摘されているように、ACE阻害薬を安易に「腎毒性薬」と呼ぶのも問題ですが、逆に「腎保護薬だから安全」と思い込むのも問題です(Clin Med 2019; 19(1): 63–68)。大切なのは、保護と障害が同じ機序の表裏だと理解することですね。
私ならまず、「腎灌流圧を下げうる他の要因が重なっていないか」を確認します。薬単体の問題ではなく、患者の全身状態とのかけ算です。ここ、迷いやすいところですが、「薬を止めるかどうか」より先に「なぜGFRが落ちたのか」を考える順番が大切です。
2. リスク因子——「この患者は大丈夫か」を判断する軸

「腎保護薬だから大丈夫」で思考が止まると、リスク因子の確認がスキップされがちです。では、どんな患者で注意が必要なのか。複数の文献を総合すると、ACE阻害薬によるAKIのリスク因子は以下のように整理できます。
| カテゴリ | 具体的なリスク因子 |
|---|---|
| 腎灌流低下 | 両側腎動脈狭窄、単腎への腎動脈狭窄、腎移植後(Hannedouche et al, Nephron 1991; Hays et al, Clin Nephrol 1983) |
| 循環血液量減少 | 脱水(嘔吐・下痢)、利尿薬併用、Na制限、低血圧(Textor SC, Semin Nephrol 1997) |
| 心機能低下 | うっ血性心不全(特に低血圧・低心拍出量)(CONSENSUS II, SOLVD試験) |
| 併用薬 | NSAIDs(PG依存性腎灌流の阻害)、K保持性利尿薬、利尿薬全般(Cooke & De Besse, Int J Clin Pharmacol Ther 1994) |
| 患者背景 | 高齢者(平均71歳:Wynckel et al, Am J Hypertens 1998)、既存のCKD、広範な動脈硬化性疾患 |
| 注意 | 用量依存性・投与期間依存性は報告されていない(Wynckel et al 1998; Textor 1997) |
ここ、心当たりありませんか。高齢の心不全患者にACE阻害薬+ループ利尿薬+NSAIDs——いわゆる「トリプルワーミー」の処方は、外来でもときどき見かけます。しかもNSAIDsはOTCで患者さんが自分で追加していることもある。処方箋だけ見ていると気づけないパターンです。
正直、全部のリスク因子を毎回チェックするのは難しくないですか?

オカメインコ

ポッポ先生
全部覚える必要はないです。まずは「腎灌流圧を下げる要因が2つ以上重なっていないか」に絞ってチェックすると現実的です。脱水+利尿薬+ACE阻害薬の3点セットは特に要注意になります。
逆に言うと、腎機能が正常でリスク因子のない高血圧患者では、臨床的に意味のあるGFR低下はまれ(0.1〜1%程度)とされています(Materson BJ, Am J Cardiol 1992; Keane et al, Ann Intern Med 1989)。ここは過度に恐れるところではありません。「腎保護薬だから安心」も「腎障害が怖いから出さない」も、どちらも極端です。必要なのは、どの患者で・どの条件が重なったら注意するか、という線引きのほうです。
3. 発症頻度と転帰——数字で見る全体像
「実際どのくらい起きるのか」という疑問は当然です。各添付文書情報および臨床試験データから報告されている発症率を整理します。
| 薬剤名 | 発症率 | 備考 |
|---|---|---|
| ベナゼプリル | 2% | ベースラインSCrの50%以上上昇 |
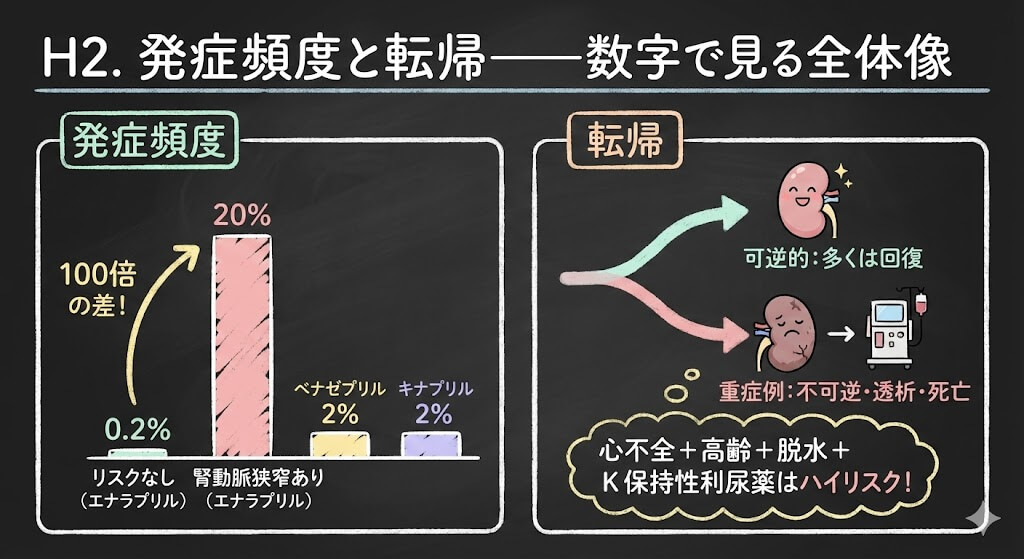
| エナラプリル | 0.2〜20% | 高血圧(リスク因子なし)0.2%、腎動脈狭窄あり20%(Schwartz et al 1991) |
| モエキシプリル | 1〜2% | 利尿薬併用で高率 |
| キナプリル | 2% | 正常上限の1.25倍以上のSCr上昇(Rosenthal et al 1996) |
| ラミプリル | 1.5% | 心筋梗塞後患者(プラセボ1.2%)(AIRE試験, Lancet 1993) |
※上記は主に海外データです。日本で使用頻度の高いACE阻害薬の国内データは別途確認が必要です。
注目すべきは、エナラプリルの数字です。リスク因子なしなら0.2%、腎動脈狭窄があれば20%。同じ薬で100倍の差がつく。この落差がそのまま、リスク評価の意味を物語っています。両側腎動脈狭窄ではさらに高く、最大38%という発症率も示唆されています(Textor, Semin Nephrol 1997)。
転帰について
多くの場合は可逆的で、薬剤中止により腎機能はベースラインに回復します。Wynckelらの前向き研究(64例、5年追跡)では、ACE阻害薬によるAKIは可逆的であり、既存のCKDの有無にかかわらず腎機能は1ヶ月以内にベースラインに回復したと報告されています(Am J Hypertens 1998)。
ただし——ここは注意が必要ですが——重度心不全で腎機能がRA系に強く依存している症例では、不可逆的な間質線維化(Textor, Semin Nephrol 1997)、透析導入(Al Shohaib & Raweily, Am J Nephrol 2000; Smith et al, Am J Nephrol 1989)、さらには死亡例も報告されています。Speirsらの大規模市販後調査では、エナラプリルによる致死的腎不全例のうち7/10例でK保持性利尿薬の併用が寄与因子として挙げられました(BMJ 1988)。
可逆的と聞くと安心しますが、致死例もあるんですね…。見極めのポイントはどこですか?

オカメインコ

ポッポ先生
「心不全+高齢+脱水+K保持性利尿薬」の組み合わせが最もハイリスクです。特にCHF患者でSCrが急上昇した場合は速やかな対応が必要になります。発症は投与開始24時間〜数日で見られるので(Al Shohaib & Raweily 2000)、導入初期のモニタリングが鍵ですね。
4. モニタリングと対応——KDIGO 2024を踏まえた判断基準
4-1. 開始時・増量時のモニタリング
KDIGO 2024ガイドラインでは、ACE阻害薬(またはARB)の開始・増量後、2〜4週間以内に血清クレアチニン(SCr)と血清カリウムを確認することが推奨されています(Practice Point 3.6.2)。
いまの状況だと、この「2〜4週間」のモニタリングが抜け落ちやすいケースがあります。特に外来で処方が出て、次回受診が2ヶ月後——という場合。「腎保護の薬だし大丈夫だろう」というイメージがあると、モニタリングの優先度が下がりがちです。でも、先ほど見た通り、ACE阻害薬開始直後こそリスクが高い時期。私ならまず処方箋を確認した時点で、「次の採血はいつですか?」と患者さんに声をかけます。
4-2. SCr上昇時の判断閾値
ここは明確な基準があります。KDIGO 2024(Practice Point 3.6.4)およびKDIGO 2022糖尿病管理ガイドラインでは、「開始または増量後4週間以内にSCrがベースラインから30%を超えて上昇した場合、AKIの精査を行うべき」とされています。
誤解されやすいので先に言うと、ACE阻害薬開始後のeGFR軽度低下(30%未満)は、輸出細動脈拡張に伴う予想される変化であり、むしろ長期的な腎保護効果のサインとも考えられています(Navis et al, Drug Saf 1996)。ここで「SCrが上がった、腎臓が悪くなっている」と早合点して中止するケースが実は現場で散見されます。腎保護の機序を「GFRが下がる方向に働く」とまで理解していれば、この軽度上昇は想定内だと判断できるはずです。
| SCr変動 | 対応 |
|---|---|
| 30%未満の上昇 | 予想される変化。継続し、経過観察。 |
| 30%以上の上昇(4週以内) | AKIの精査。脱水・併用薬(NSAIDs等)の確認。原因に応じて減量・中止を検討。 |
| 急速な上昇+乏尿 | 速やかな薬剤中止。補液、原因検索。透析の必要性を評価。 |
(KDIGO 2024 Practice Point 3.6.4 / 各一次文献を基に整理)

ポッポ先生
STOP-ACEi試験の結果も押さえたいところです。eGFRが30未満に低下した患者でも、ACE阻害薬の中止は腎・心血管アウトカムの改善につながらなかったとされています。「腎機能が落ちたからとりあえず中止」は、かえって患者の不利益になりうるんですね。
ただし、eGFRが15未満の場合はACE阻害薬の新規開始を支持するエビデンスがない点にも注意が必要です(KDIGO 2024)。すでに服用中で安定している場合は継続可能ですが、新規導入は慎重に判断してください。
5. シックデイ対応——急性疾患時の一時休薬ルール
現場だとここで詰まりがちです。ACE阻害薬を服用中の患者が発熱・嘔吐・下痢などの急性疾患にかかったとき、薬を一時的に休薬すべきかどうか。
「腎保護の薬だから飲み続けたほうがいい」と患者さんが考えていることもあります。それどころか、私たち薬剤師のほうが「止めて大丈夫だろうか」と躊躇してしまうこともある。ここは、保護と障害の両面を理解していないと判断が揺れやすいところです。
NICEガイドラインおよび国際的なDelphi合意(Consensus Recommendations, Am J Kidney Dis 2023)では、脱水リスクのある急性疾患時にACE阻害薬(およびARB・利尿薬・NSAIDs・メトホルミン・SGLT2阻害薬)の一時休薬が推奨されています。カナダ糖尿病学会のSADMANS(Sulfonylurea, ACEi, Diuretics, Metformin, ARB, NSAIDs, SGLT2i)という覚え方も知られています。
5-1. 一時休薬の判断基準
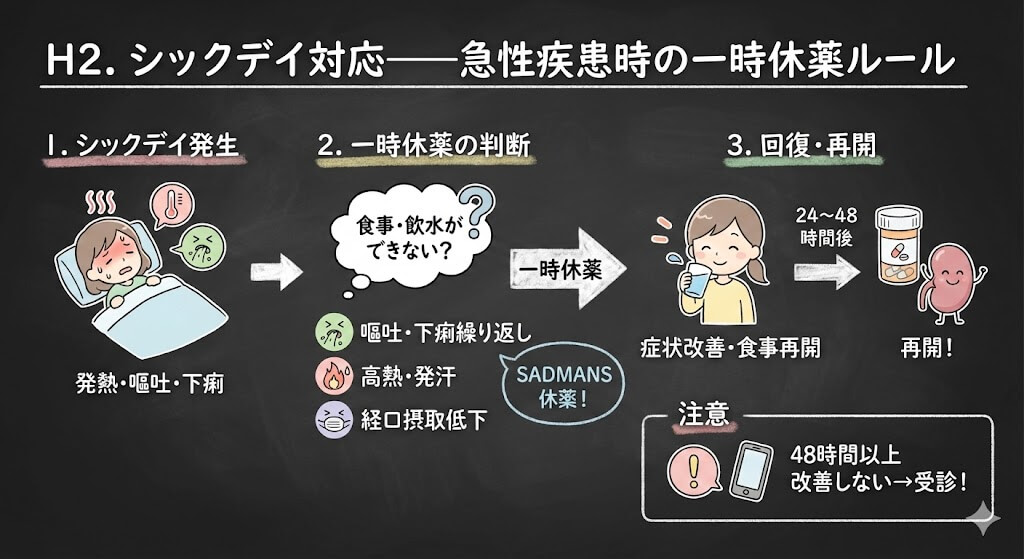
しないほうが安全なのは、「軽い風邪で食事・飲水が普通にできている」場合に慌てて休薬すること。逆に、以下の症状がある場合は一時休薬を検討します:
- 嘔吐や下痢が繰り返し起きている
- 高熱で発汗が多い
- 経口摂取が著しく低下している
- 低血圧の兆候がある
でも、患者さんに「自分で薬を止めていい」と伝えるのは怖くないですか? 心不全の人がACE阻害薬を止めたら悪化しそうで…

オカメインコ

ポッポ先生
その懸念は正当です。実際、AKI後にACE阻害薬を再開しなかった群のほうが死亡率が上昇したという観察研究もあります(Brar et al, JAMA Intern Med 2018)。だからこそ、「止める判断」と「再開する判断」をセットで伝えることが大事ですね。
5-2. 再開のタイミング
一般的には、症状が改善し食事・飲水が24〜48時間正常に戻った時点で再開が目安です。2024年の大規模コホート研究(Kidney Int Rep 2024)では、AKI後の早期再開群のほうが死亡率・心血管イベント・透析導入リスクが低く、高K血症や再AKIのリスク増加はなかったと報告されています。
ただし、これは観察研究のデータであり、個別の患者状態によって判断は異なります。不確実な点も残る領域であることは明記しておきます。
どうですか? 「止めるルール」だけでなく「戻すルール」まで患者さんに説明できていますか。ここまでカバーできると、薬剤師としてのシックデイ指導の質がぐっと上がります。
6. 薬剤師の実務——処方鑑査から患者指導まで
6-1. まず自分の「認知の偏り」を確認する
少し立ち止まって考えてみてください。ACE阻害薬の処方を見たとき、頭の中で自動的に走るチェックリストは何でしょうか。
「空咳の既往は?」「妊娠の可能性は?」「K値は?」——ここまで浮かぶ方は多いと思います。でも「腎灌流圧が維持できている患者か?」まで浮かぶでしょうか。
これは知識の有無というより、どのフレームで薬を捉えているかの問題です。ACE阻害薬を「腎保護薬」としてだけ認識していると、AKIリスクの確認が自然とチェックリストから抜け落ちます。「良い薬」のイメージが、盲点をつくるわけです。
6-2. 処方鑑査のチェックポイント
私ならまずこの4点から確認します:
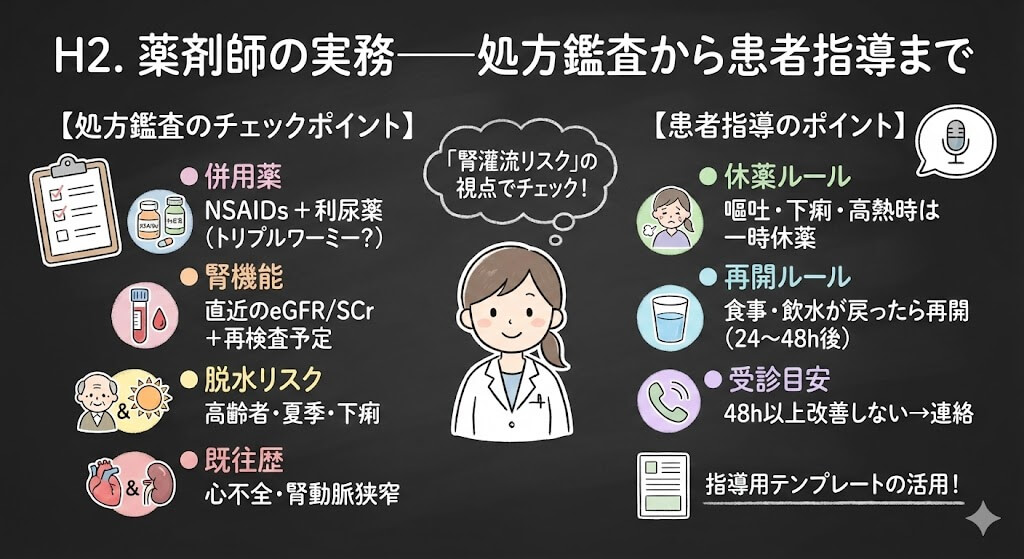
- 併用薬:NSAIDs(OTC含む)+利尿薬+ACE阻害薬のトリプルワーミーがないか
- 腎機能:直近のeGFR/SCr。ACE阻害薬開始・増量後の再検査が予定されているか
- 脱水リスク:高齢者、夏季、下痢症状の有無。利尿薬の用量
- 既往歴:腎動脈狭窄の有無、心不全の重症度、糖尿病の合併
6-3. 患者指導のポイント
シックデイルールについては、「元気なときに」伝えておくのが鉄則です。実際、英国の調査ではシックデイ指導を受けていた患者はわずか18%だったという報告があります(BMC Nephrol 2024)。
伝えるべき内容は3つに絞ると現実的です:
- 嘔吐・下痢・高熱で食事がとれないときは、一時的に服用を控える
- 食事・飲水が普通に戻ったら再開する(目安:24〜48時間)
- 48時間以上改善しなければ、医師・薬剤師に連絡する
OTCのNSAIDsまでチェックするのは現実的ですか? 時間がないんですが…

オカメインコ

ポッポ先生
全患者に毎回は難しいです。ただ、ACE阻害薬+利尿薬の併用がある患者に絞れば対象は限定できます。そういう方に「市販の痛み止めは使いますか?」と一言聞くだけでも、トリプルワーミーの予防になります。
もうひとつ、患者さん側の認識にも触れておきます。患者さんが「この薬は腎臓を守る薬ですよ」とだけ説明されていると、体調が悪くても「腎臓のために飲み続けなきゃ」と考えることがあります。シックデイの説明は、患者さんの認識のアップデートでもあるんです。「普段は腎臓を守ってくれる薬ですが、脱水のときは一時的に腎臓に負担がかかることがあります」——この一言があるだけで、休薬指導の受け入れがまったく変わります。
まとめ——「腎保護薬」の裏側を知ることが、本当の腎保護になる
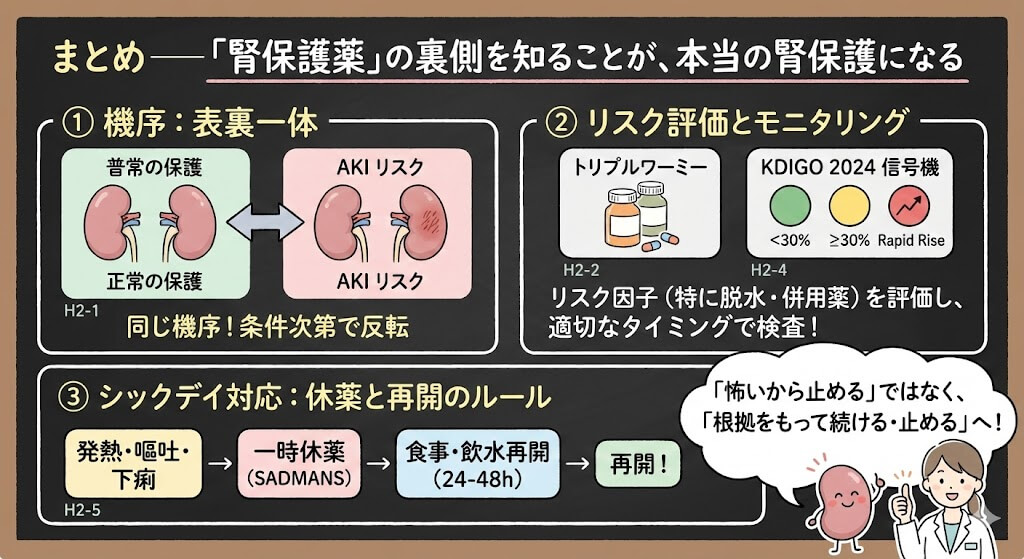
ここまでの内容を整理します。ACE阻害薬によるAKIは、①腎灌流圧低下+②輸出細動脈拡張阻害、という「条件の重なり」で起こる薬理学的な延長線上の事象です。腎保護と腎障害は、同じメカニズムの表と裏です。薬そのものの毒性ではありません。
だからこそ、薬剤師に求められるのは「止めるか続けるか」の二択ではなく、リスク因子の評価とモニタリングの設計です。「腎保護薬だから大丈夫」でも「腎障害が怖いから出さない」でもなく、どの条件で保護から障害に反転するかを見極めること。これが、ACE阻害薬の恩恵を安全に届けるための薬剤師の仕事です。
次の一歩として:
- いま担当している患者のうち、ACE阻害薬+利尿薬+高齢者のトリオに該当する方が何人いるか、確認してみてください
- 自分の処方鑑査のチェックリストに「腎灌流リスク」が入っているか、振り返ってみてください
- シックデイ指導のテンプレート(休薬対象薬リスト+再開基準+連絡先)を薬局内で共有できると、指導の質と効率が上がります
- KDIGO 2024ガイドラインの日本語要約や、日本腎臓学会のCKD診療ガイドは一次情報として確認しておくと安心です

ポッポ先生
「腎保護薬」の裏側まで理解して初めて、本当の意味で腎臓を守れます。「怖いから止める」ではなく、「根拠をもって続ける・止める」を目指しましょう。
参考文献
- Textor SC. Renal failure related to angiotensin-converting enzyme inhibitors. Semin Nephrol. 1997;17(1):67-76.
- Wynckel A, Ebikili B, Melin J-P, et al. Long-term follow-up of acute renal failure caused by angiotensin converting enzyme inhibitors. Am J Hypertens. 1998;11:1080-1086.
- Materson BJ. Adverse effects of angiotensin-converting enzyme inhibitors in antihypertensive therapy with focus on quinapril. Am J Cardiol. 1992;69:46C-53C.
- Keane WF, Polis A, Wolf D, et al. The long-term tolerability of enalapril in hypertensive patients with renal impairment. Nephrol Dial Transplant. 1997;12(suppl 2):75-81.
- Navis G, Faber HJ, de Zeeuw D, et al. ACE inhibitors and the kidney: a risk-benefit assessment. Drug Saf. 1996;15:200-211.
- Speirs CJ, Dollery CT, Inman WHW, et al. Postmarketing surveillance of enalapril II. BMJ. 1988;297:830-832.
- Al Shohaib S, Raweily E. Acute tubular necrosis due to captopril. Am J Nephrol. 2000;20(2):149-152.
- Smith WR, Neill J, Cushman WC, et al. Captopril-associated acute interstitial nephritis. Am J Nephrol. 1989;9:230-235.
- Cooke HM, De Besse A. Angiotensin converting enzyme inhibitor-induced renal dysfunction: recommendations for prevention. Int J Clin Pharmacol Ther. 1994;32:65-70.
- Kostis JB, Shelton B, Gosselin G, et al. Adverse effects of enalapril in the studies of left ventricular dysfunction (SOLVD). Am Heart J. 1996;131:350-355.
- KDIGO 2024 Clinical Practice Guideline for the Evaluation and Management of CKD. Kidney Int. 2024;105(4S):S117-S314.
- KDIGO 2022 Clinical Practice Guideline for Diabetes Management in CKD. Kidney Int. 2022;102(5S):S1-S127.
- Consensus Recommendations for Sick Day Medication Guidance. Am J Kidney Dis. 2023;81(5):564-574.
- Brar S, Ye F, James MT, et al. Association of ACEi/ARB Use With Outcomes After AKI. JAMA Intern Med. 2018;178(12):1681-1690.
- Lam NN, et al. Impact of Different ACEi/ARB Resumption Timing on Post-AKI Outcomes. Kidney Int Rep. 2024.
- Acute kidney injury and ‘nephrotoxins’: mind your language. Clin Med. 2019;19(1):63-68.
- Hannedouche T, Godin M, Fries D, et al. Acute renal thrombosis induced by angiotensin-converting enzyme inhibitors in patients with renovascular hypertension. Nephron. 1991;57:230-231.
- DiBianco R. Adverse reactions with angiotensin converting enzyme (ACE) inhibitors. Med Toxicol. 1986;1:122-141.
※日本国内での適用にあたっては、各薬剤の最新添付文書、日本腎臓学会CKD診療ガイド、日本高血圧学会ガイドライン等を併せてご確認ください。