2025年12月、厚生労働省がタミフル(オセルタミビル)とイナビル(ラニナミビル)のスイッチOTC化に関するパブリックコメントの募集を開始しました。抗インフルエンザ薬の市販化が実現すれば、国内では初めてのケースです。
正直に言うと、私はこの議論を見ながら「耐性化が心配だからダメ」という意見に100%は乗れずにいます。調剤薬局で働いていて、インフルエンザシーズンの外来混雑を毎年見ているからです。2時間待って検査して、陽性だったら処方箋もらって、薬局でまた30分以上待つ。この流れ、本当にベストなんでしょうか。
この記事では、最新のエビデンスを整理しながら、「抗インフルエンザ薬の効果は限定的だけど、だからこそOTC化も選択肢としてアリなのでは」という、ちょっと逆説的な視点で考えてみます。
目次
そもそも抗インフルエンザ薬の効果ってどのくらい?——最新メタアナリシスが示す現実
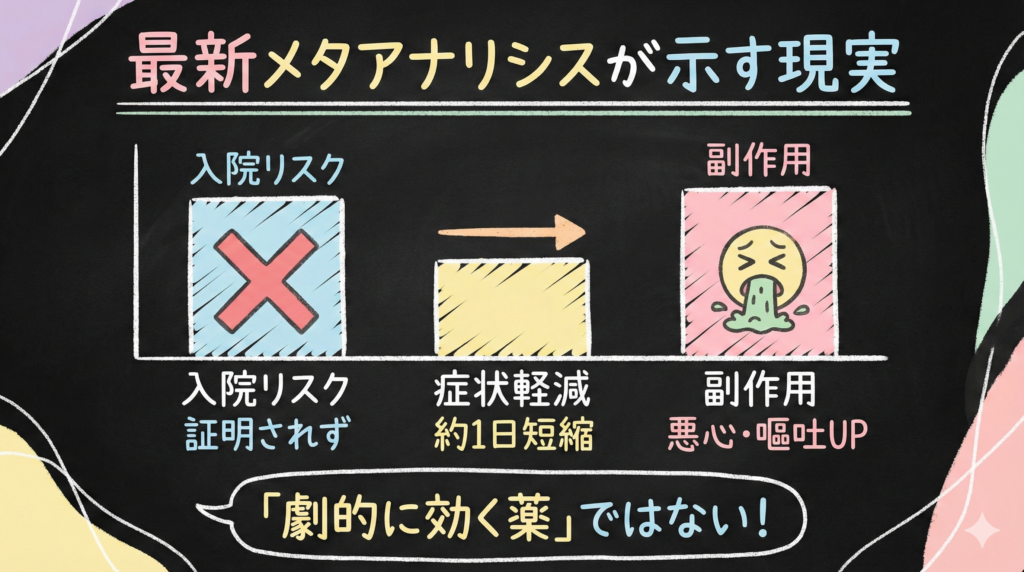
ここ、誤解されやすいので先に言うと、タミフルは「飲めば劇的に良くなる薬」ではありません。
JAMA Internal Medicine 2024年メタアナリシス:入院リスク低減は証明されず
2024年にJAMA Internal Medicineに掲載されたHanulaらのメタアナリシスでは、15件のランダム化比較試験(6,166人)を解析し、外来インフルエンザ患者におけるオセルタミビルの効果を検証しています。
| 項目 | 結果 |
|---|---|
| 入院リスク | RR 0.79(95%CI: 0.48-1.29)=有意差なし |
| 高リスク患者の入院 | RR 0.85(95%CI: 0.40-1.82)=有意差なし |
| 65歳以上の入院 | RR 1.01(95%CI: 0.21-4.90)=有意差なし |
| 悪心 | RR 1.43(95%CI: 1.13-1.82)=増加 |
| 嘔吐 | RR 1.83(95%CI: 1.28-2.63)=増加 |
つまり、入院予防効果は統計的に証明されず、一方で消化器系の副作用は増えるという結果でした。
え、じゃあ飲んでも意味ないってこと?

オカメインコ

ポッポ先生
そこまで単純ではないです。症状が軽減するまでの時間は約17〜25時間短縮されるという報告があります。ただ、これが臨床的に意味のある差かどうかは議論があるところです。
JAMA Internal Medicine 2025年ネットワークメタアナリシス:さらに厳しい評価
2025年1月に発表されたGaoらの大規模ネットワークメタアナリシス(73試験、34,332人)では、複数の抗インフルエンザ薬を比較検討しています。
オセルタミビルの評価:
- 低リスク患者の入院率:変化なし(高い確実性)
- 高リスク患者の入院:ほとんど効果なし(高い確実性)
- 症状軽減:1日未満の短縮(臨床的に重要でない可能性)
- 副作用:悪心・嘔吐が増加(中程度の確実性)
バロキサビル(ゾフルーザ)の評価:
- 高リスク患者の入院:減少の可能性(低い確実性)
- 症状軽減:約1日短縮
- 副作用:増加なし(高い確実性)
- ただし約10%で薬剤耐性出現の可能性
どうですか? 「絶対に必要な薬」というより「あったら少し楽になるかもしれない薬」という位置づけが見えてきませんか。
「効果が限定的」だからこそOTC化が選択肢になる——逆説的な論理
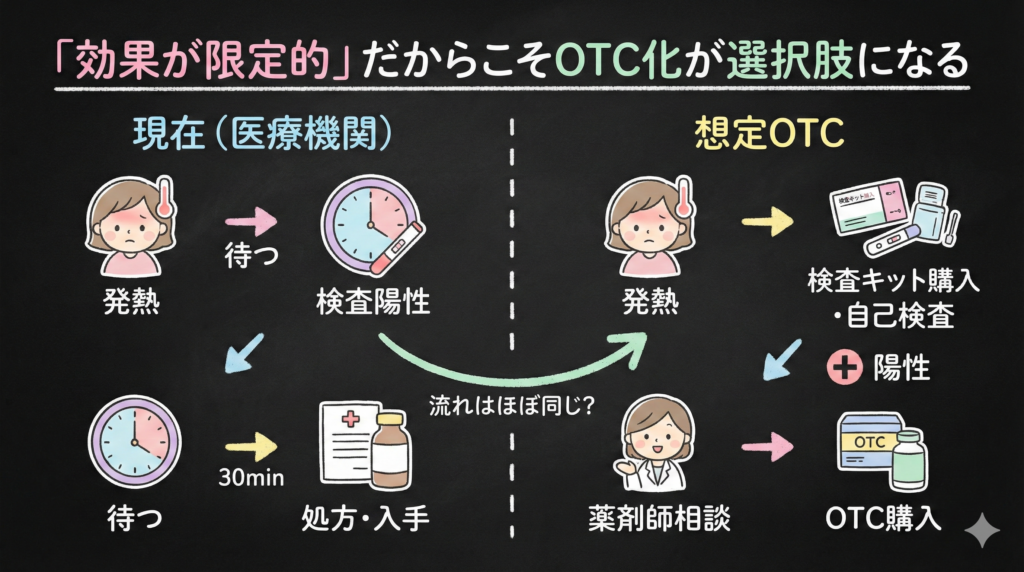
ここで私の考えを述べます。
「効果が限定的な薬をわざわざOTC化する意味があるのか」という批判があります。確かに一理ある。でも、逆に言うと、効果が限定的だからこそ、医療機関を必ず受診しなければならない理由も弱いのではないでしょうか。
日本の現状:検査→陽性→処方という流れ
日本では、インフルエンザが疑われたらまず医療機関で迅速検査を受けます。陽性なら抗インフルエンザ薬が処方される。この流れ、ほぼ自動的ですよね。
いまの状況だと、こんなシナリオが典型的です:
- 発熱(38度超え)で発症
- 翌朝、発熱外来へ(待合室で2時間)
- 迅速検査で陽性
- 処方箋をもらう
- 薬局へ(さらに30分〜1時間待ち)
- やっとタミフル入手
この間、体調不良のまま何時間も待つわけです。しかも、インフルエンザの症状がピークの時期に。
でも、医師の診察が必要なんじゃないですか? 他の病気の可能性もあるし…

オカメインコ

ポッポ先生
その通り、重症化リスクの判断は重要です。ただ、現実には多くの外来で「検査陽性→処方」がほぼ自動的に行われています。医師の診察が形骸化しているケースも少なくない。だったら、薬局で検査キット+陽性なら購入という仕組みにしても、本質的には変わらないのでは、という議論はあり得ます。
テスト・アンド・トリート方式の可能性
もしOTC化が実現するなら、おそらく「薬局で検査キットを購入→陽性なら抗インフルエンザ薬を購入」という形になるでしょう。これ、冷静に考えると、現在の医療機関での流れと大きな差はありません。
| 方式 | 流れ |
|---|---|
| 現行(医療機関) | 検査 → 陽性 → 処方 → 薬局で調剤 |
| 想定されるOTC方式 | 検査キット購入 → 自己検査 → 陽性 → 薬剤師相談 → OTC購入 |
心当たりありませんか? 「医師の診察」と言っても、インフルエンザ確定後に詳細な診察が行われるケースは実際には多くない。検査結果を見て処方箋を書く、という流れが大半です。
耐性化リスク:「使いすぎ=耐性」は単純すぎる

OTC化反対派の最大の懸念は耐性化です。私ならまず確認したいのは、「本当に使用量と耐性化は直結するのか」という点です。
日本のタミフル使用量は世界一、でも耐性率は低かった
2007〜2009年の季節性H1N1型でオセルタミビル耐性株(H275Y変異)が世界的に流行しました。
| 国 | 耐性率 | タミフル使用量 |
|---|---|---|
| ノルウェー | 67% | 少ない |
| フランス | 47% | 中程度 |
| 米国 | 10%以上 | 中程度 |
| 日本 | 2.6% | 世界最多 |
驚くべきことに、世界のタミフル消費量の約7〜8割を占める日本で、耐性率は欧州より低い水準でした。
それって矛盾してますよね?

オカメインコ

ポッポ先生
この耐性株は、薬剤選択圧とは無関係に自然発生的に出現したものでした。NEJMのMoscona論文(2009)では、HAタンパク質の補償変異との共選択によって、伝播力を維持したまま耐性を獲得した可能性が指摘されています。つまり、「使いすぎ=耐性」という単純な図式は成り立たなかったんです。
ただし、油断は禁物
もちろん、これは「耐性を気にしなくていい」という意味ではありません。
2023-2024年の動向:
- I223V/S247N二重変異株が欧州を中心に検出(オセルタミビル感受性13〜16倍低下)
- 2024年9月、横浜の小学校でNA H275Y変異株のアウトブレイク発生
(出典:CDC EID 2024;30(7)、Euro Surveill 2024)
2025年1月時点の日本国内サーベイランスでは、治療前検体からオセルタミビル耐性変異は検出されていませんが、継続的な監視は必要です。
逆に言うと、OTC化によってサーベイランス体制が弱体化することが問題であり、「使用量が増えること」自体が直接的なリスクとは限らない。ここ、迷いやすいところです。
海外で使われていない理由——日本の「国民性」問題

海外、特に欧米では抗インフルエンザ薬の使用は日本ほど一般的ではありません。
WHOの推奨
WHOは抗インフルエンザ薬を「重症患者または重症化リスクの高い患者」に推奨しています。健康な成人が軽症のインフルエンザで必ず抗ウイルス薬を飲む、という文化は日本特有です。
なぜ日本では使われるのか
私なりの仮説ですが、いくつかの要因があると思います。
1. 「1日早く治る」の価値が高い社会
日本では、病欠への風当たりが強い。「少しでも早く職場に復帰したい」「子どもの学校を休ませたくない」という圧力がある。たった1日の短縮でも、社会的には大きな価値がある。
2. 医療アクセスの良さと医療費の安さ
3割負担で医師の診察を受けられ、抗インフルエンザ薬も比較的安価に入手できる。このアクセスの良さが「とりあえず受診」「とりあえず処方」を促進している。
3. 「何かしたい」心理
インフルエンザで苦しいとき、「何か薬を飲んでいる」という安心感は馬鹿にできない。プラセボ効果も含めて、主観的な満足度には寄与している可能性がある。
それって、薬として意味があるかどうかとは別の話ですよね…

オカメインコ

ポッポ先生
その通り。でも、医療は科学だけでは完結しない。患者さんの満足度や安心感も、広い意味での「治療効果」の一部と捉えることもできます。もちろん、それを理由に過剰処方を正当化すべきではないですが。。。
医療機関の混雑という現実問題

ここ、現場だと本当に深刻です。
インフルエンザシーズンの発熱外来
毎年12月〜2月、発熱外来はパンク状態になります。私が働く薬局の近くのクリニックでは、ピーク時には3時間待ちも珍しくない。
この状況で何が起きているか:
- 医療者の疲弊:1日100人以上の発熱患者を診る医師もいる
- 待合室での感染拡大:具合の悪い人が密集して待つ
- 48時間ルールとの矛盾:抗インフルエンザ薬は発症48時間以内が効果的なのに、受診できない
- 軽症者と重症者の選別困難:本当に医師の診察が必要な人が埋もれる
もしOTC化によって軽症の成人が薬局で完結できれば、医療機関の負担は確実に減ります。
m3.comの調査結果
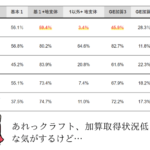
医療者向けサイトm3.comの調査では、タミフルOTC化への賛否が分かれています。
| 職種 | 賛成 | 反対 |
|---|---|---|
| 開業医 | 42.2% | 57.8% |
| 勤務医 | 61.1% | 38.9% |
| 薬剤師 | 50.6% | 49.4% |
勤務医の賛成率が高いのは注目に値します。病院の発熱外来で疲弊している医師たちは「どうにかしてほしい」と思っている。一方、開業医は「患者が来なくなる」という経営面の懸念もあるかもしれません(これは推測ですが)。
自己判断のリスク——でも本当に「医師の診察」で防げているか?

OTC化反対の論拠として、「自己判断による他疾患の見逃しリスク」があります。これは確かに重要な論点です。
小児の診断精度:医師でも38%
フィンランドの研究(Peltola V, et al. Clin Infect Dis. 2005)では、小児科医の臨床診断でもインフルエンザの感度は38%でした。検査なしでは6割以上が外れる。
これを根拠に「だから医師の診察が必要」と言う人がいます。でも、待ってください。
現実の診療フロー:
- 問診(発熱、咳、関節痛など)
- 迅速検査
- 陽性なら処方
この流れで、「医師の診察」が果たしている役割は何でしょうか。迅速検査の前後で、詳細な身体診察が行われているケースはどれくらいあるでしょうか。
でも、検査が陰性でも他の病気を疑って診察してくれるんじゃ…

オカメインコ

ポッポ先生
理想はそうです。でも、混雑した発熱外来で、1人あたり5分の診察時間で、どこまでできるか。現実には「陰性でした、様子を見てください」で終わるケースも多い。薬剤師が「陰性でも重症感があれば受診を」と伝えるのと、本質的にどれだけ違うか、冷静に考える必要があります。
重症化サインの判断
OTC化が実現する場合、薬剤師が確認すべき「重症化サイン」は明確にできます:
- 呼吸困難・息切れ
- 意識障害・けいれん
- 脱水症状(尿が出ない、口の渇き)
- 胸痛
- 症状が一度改善した後の再悪化
これらがある場合は、検査結果に関わらず医療機関受診を勧める。このスクリーニングは、適切な研修を受けた薬剤師なら十分に可能です。
ニュージーランドの先行事例——5年間で問題なし
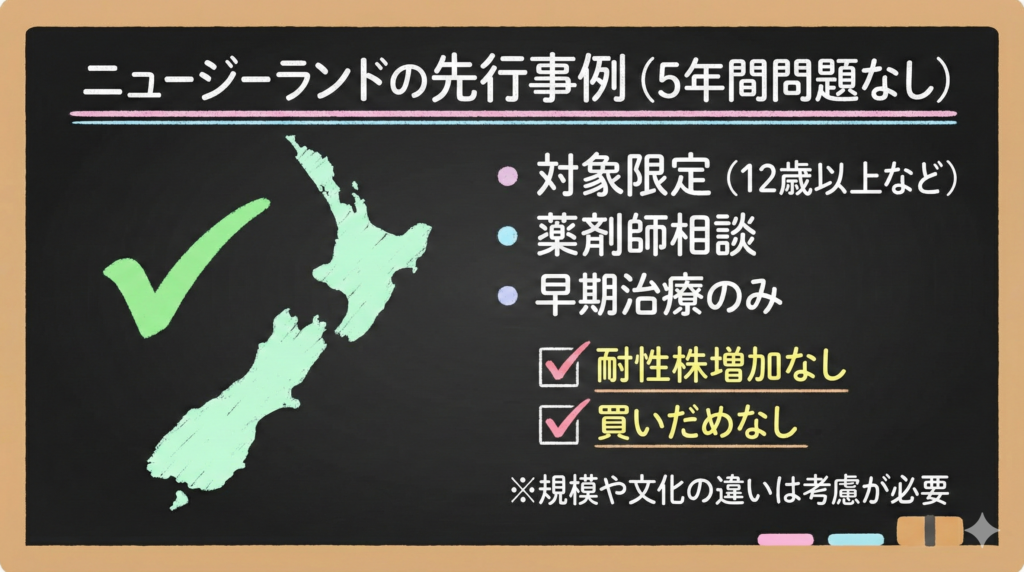
ニュージーランドは2007年から世界で唯一、オセルタミビルの薬剤師供給(処方箋なし)を認めています。
供給条件
- インフルエンザシーズン(5〜9月)のみ
- 12歳以上
- 薬剤師との対面相談必須
- 発症早期の治療目的に限定
5年間の追跡結果(Gauld NJ, et al. J Antimicrob Chemother. 2012)
| 項目 | 結果 |
|---|---|
| 耐性株の増加 | 認められず |
| ワクチン接種率への影響 | なし |
| 買いだめ問題 | 発生せず |
| 薬剤師供給の割合 | 全供給の11〜31%(残りは処方箋) |
ただし、ニュージーランドの人口は約500万人。日本の約1億2,000万人とは規模が違います。また、薬剤師からは「ルールが複雑で運用しにくい」という声も出ています。
日本で同じ結果になる保証はありませんが、「厳格な条件下なら運用可能」という先行事例ではあります。
私が考える「現実的な落としどころ」
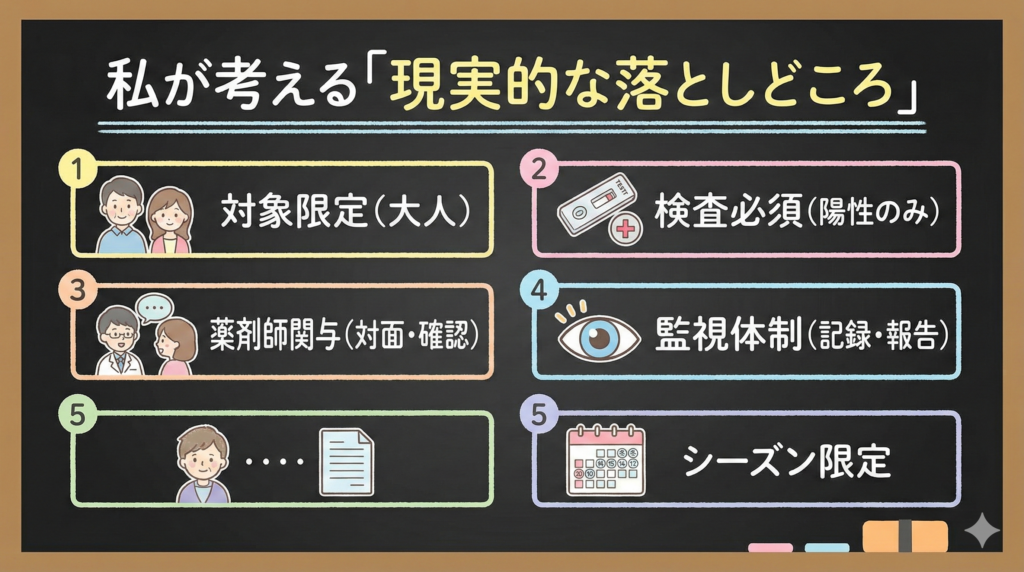
ここまで整理してきて、私なりの結論です。
OTC化の条件
1. 対象の限定
- 成人(18歳以上)に限定
- 小児、高齢者(65歳以上)、妊婦、基礎疾患のある方は除外→医療機関受診を推奨
2. テスト・アンド・トリート方式
- 薬局での迅速検査キット使用(または自己検査結果の提示)
- 陽性確認後のみ販売
3. 薬剤師の関与
- 対面での問診必須
- 重症化サインのスクリーニング
- 発症48時間以内の確認
4. サーベイランス体制の維持
- OTC販売の記録・報告義務
- 耐性監視のための検体収集システム
5. シーズン限定
- インフルエンザ流行期のみの販売
しないほうが安全なこと
- 小児への販売(診断精度の問題、異常行動リスク)
- 予防目的での販売
- ネット販売(対面確認ができない)
まとめ:便利さと安全のバランスを考える
抗インフルエンザ薬のOTC化は、単純に「良い・悪い」で割り切れる問題ではありません。
認めるべき事実:
- 抗インフルエンザ薬の効果は限定的(症状軽減約1日、入院予防効果は証明されず)
- 日本の医療機関はインフルエンザシーズンに深刻な混雑状態
- 現行の「医師の診察」は多くの場合、検査結果に基づく処方に留まっている
- 耐性化リスクは「使用量」だけでは決まらない
- ニュージーランドでは5年間、問題なく運用されている
慎重に考えるべき点:
- 小児の診断・治療は医療機関で行うべき
- サーベイランス体制の維持は必須
- 薬剤師の適切な関与が安全の鍵
- 日本特有の「とりあえず薬」文化への対応
「効果が限定的な薬だから、OTC化は無意味」ではなく、「効果が限定的な薬だからこそ、わざわざ医療機関を経由する必要性も限定的」——この視点も、議論のテーブルに載せていいのではないでしょうか。
パブリックコメントの募集期限は2026年1月8日です。賛成・反対、どちらの立場であっても、現場を知る薬剤師として意見を表明する機会です。
確認先(一次情報)
効果に関するエビデンス
- Hanula R, et al. Evaluation of Oseltamivir Used to Prevent Hospitalization in Outpatients With Influenza: A Systematic Review and Meta-Analysis. JAMA Intern Med. 2024;184(1):18-27.
- Gao Y, et al. Antiviral Medications for Treatment of Nonsevere Influenza: A Systematic Review and Network Meta-Analysis. JAMA Intern Med. 2025;185(3):293-301.
耐性に関する文献
- Ujike M, et al. Oseltamivir-Resistant Influenza Viruses A (H1N1) during 2007–2009 Influenza Seasons, Japan. Emerg Infect Dis. 2010;16(6):926-935.
- Moscona A. Global Transmission of Oseltamivir-Resistant Influenza. N Engl J Med. 2009;360:953-956.
パブリックコメント・制度関連
海外のOTC状況に関する文献
- Gauld N, Kelly F, Shaw J. Is non-prescription oseltamivir availability under strict criteria workable? A qualitative study in New Zealand. J Antimicrob Chemother. 2011;66(1):201-204.
- Gauld NJ, et al. Five years of non-prescription oseltamivir: effects on resistance, immunization and stockpiling. J Antimicrob Chemother. 2012;67(12):2949-2957.
診断精度に関する論文
- Peltola V, Reunanen T, Ziegler T, et al. Accuracy of Clinical Diagnosis of Influenza in Outpatient Children. Clin Infect Dis. 2005;41(8):1198-1200.
迅速検査に関するCDCガイダンス
耐性監視に関する文献
- CDC:Influenza Antiviral Drug Resistance
- Ujike M, et al. Oseltamivir-Resistant Influenza Viruses A (H1N1) during 2007–2009 Influenza Seasons, Japan. Emerg Infect Dis. 2010;16(6):926-935.
- Moscona A. Global Transmission of Oseltamivir-Resistant Influenza. N Engl J Med. 2009;360:953-956.
- Leung NHL, et al. Global emergence of neuraminidase inhibitor-resistant influenza A(H1N1)pdm09 viruses with I223V and S247N mutations. Lancet Microbe. 2024.
- CDC EID:Multicountry Spread of Influenza A(H1N1)pdm09 Viruses with Reduced Oseltamivir Inhibition, May 2023–February 2024
- Zhang L, et al. A primary oseltamivir-resistant mutation in influenza hemagglutinin and its implications for antiviral resistance surveillance. Nat Commun. 2025.
日本国内のサーベイランス
- 新潟大学:2023-2024年シーズンの日本におけるインフルエンザサーベイランスの概要(2024年12月25日作成)
日本の診療指針